Annons
Annons
Få tillbud anmäls till Läkemedelsverket

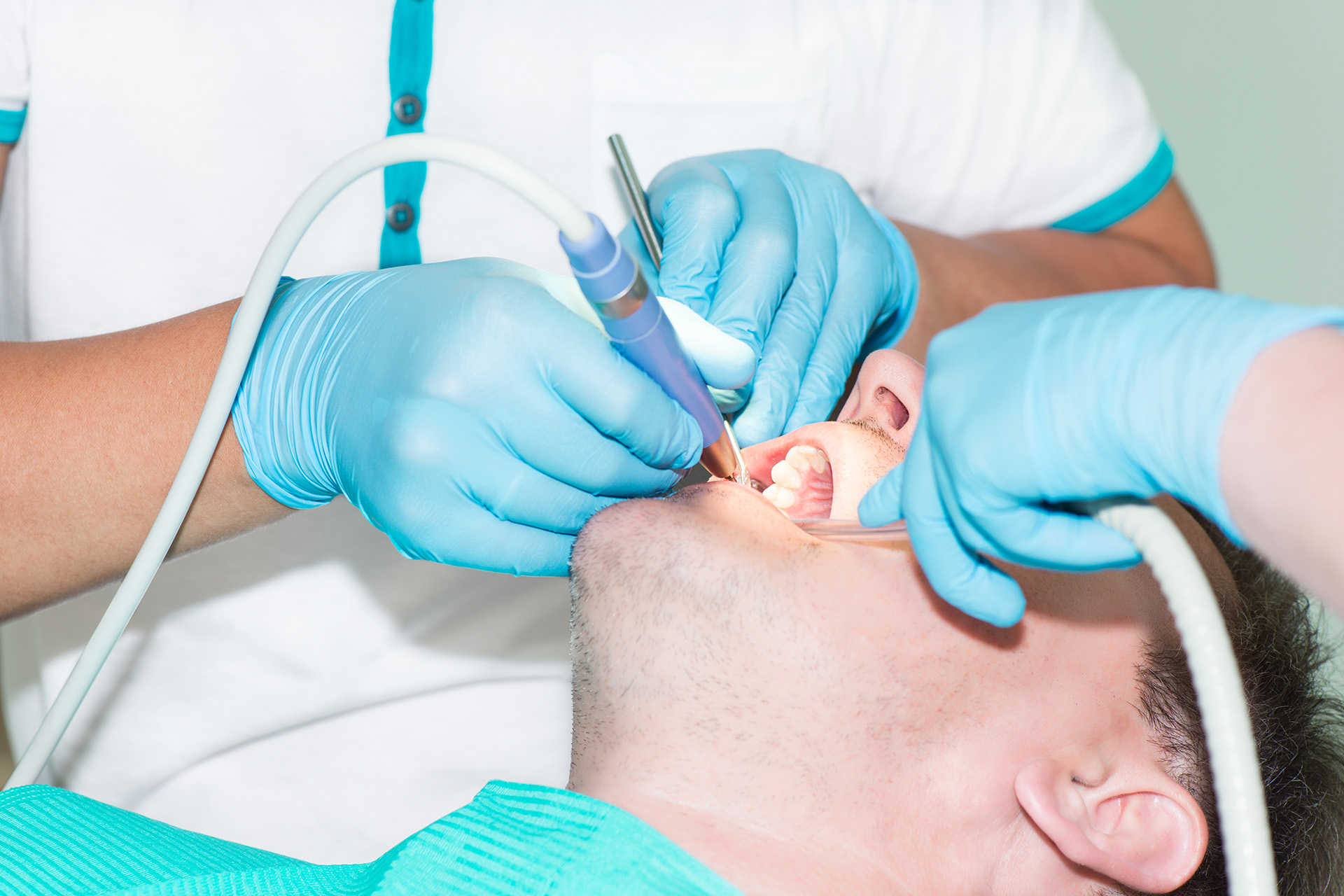
Foto: Colourbox
Det sker en underrapportering av negativa händelser med medicintekniska produkter inom tandvården. Den bedömningen gör Läkemedelsverket, som nu uppmanar tandläkare att anmäla alla negativa händelser och tillbud som rör medicintekniska produkter.

Henrik Johansson
– Det är inte klart var man ska lägga nivån i dagsläget, men vi ser helst att alla negativa händelser och tillbud som lett till försämrad hälsa eller skulle kunna leda till försämrad hälsa rapporteras. Vi vill inte att tandläkarna sållar själva. Om det betyder att vi får in tusen anmälningar från tandvården får vi hantera det, säger Henrik Johansson, utredare på Läkemedelsverket.
Det finns 800 000 olika medicintekniska produkter inom sjukvården på den europeiska marknaden. Enligt EU-förordningen MDR 2017/745 har tillverkarna ansvaret för att alla krav som ställs på dem är uppfyllda när de släpps ut på marknaden. Tillverkarens ansvar innebär till exempel att de ska utvärdera information från användarna när det gäller hur produkten används och fungerar.
Även vårdgivarna har ansvar för säkerheten. När en negativ händelse eller ett tillbud inträffar har vårdgivaren en skyldighet att anmäla det till tillverkaren och Läkemedelsverket. Ett tillbud kan till exempel vara en fil som går av och fastnar i tanden hos en patient. Det kan även vara fyllnadsmaterial som orsakar en allergisk reaktion hos en patient. Det kan även vara ett bildsystem som havererar och där röntgenbilder går förlorade.
Hittills har det inte kommit in särskilt många anmälningar från tandvården, därför misstänker Läkemedelsverket att det sker en underrapportering. Nu uppmanar Läkemedelsverket tandläkare att anmäla alla negativa händelser och tillbud som kunde ha lett till tillfälliga eller permanenta skador hos patienter och användare. Syftet är få kunskap om hur händelser som kan leda till tillfälliga och permanenta skador hos patienter ska undvikas. Rapporteringen ger även tillverkaren kunskap om hur produkten fungerar kliniskt.
En negativ händelse måste följas av en grundlig utredning och den ska påbörjas omgående. Det framgår av Socialstyrelsens föreskrifter om användning av medicintekniska produkter i hälso- och sjukvården. Det ligger även stort ansvar på tillverkaren. Varje anmäld händelse måste utredas grundligt och därför är det viktigt att tillverkaren i ett tidigt skede får kännedom om händelsen.
Enligt Läkemedelsverket ska inte vårdgivare utgå från att de själva gjort fel när en negativ händelse eller ett tillbud inträffar. Samma tillbud kan mycket väl inträffa hos andra vårdgivare om det finns ett fel hos produkten.
- Av Socialstyrelsens föreskrifter HSLF-FS 2021:52 kapitel 5 framgår hur en vårdgivare ska gå till väga vid en negativ händelse hos en medicinteknisk produkt.
- Det är Läkemedelsverket som har tillsynsansvaret för medicintekniska produkter. Anmälan görs på följande webbadress: https://www.lakemedelsverket.se/sv/rapportera-biverkningar/medicinteknik
- Enligt Socialstyrelsens föreskrifter HSLF-FS 2021:52 §5 kapitel 5 ska en anmälan till göras vid funktionsfel och försämring av en produkts egenskaper eller prestanda samt vid felaktigheter och brister i märkning eller bruksanvisning som kan leda till eller har lett till
- en patients, en användares eller någon annan persons död, eller
- en allvarlig försämring av en patients, en användares eller någon annan persons hälsotillstånd.
- Tillverkaren gör sin anmälan på följande webbadress: https://www.lakemedelsverket.se/sv/medicinteknik/folj-upp-anvandning/rapportering-av-allvarliga-tillbud#hmainbody6
- Definitionen av ett tillbud eller ett allvarligt tillbud återfinns i EU-förordningen MDR 2017/745 artikel 2, regel 64–65.

Ellenor Winquist
– Det är bra om vi får signaler från två håll, det vill säga tillverkaren och vårdgivaren, när det inträffat en negativ händelse, säger Ellenor Winquist, utredare vid Läkemedelsverket.
Så vad kan Läkemedelsverket göra efter att en negativ händelse har anmälts? Efter att tillverkaren utrett händelsen tittar Läkemedelsverket på risken med den medicintekniska produkten. Sedan undersöker man om tillverkarens utredning är tillräcklig. Läkemedelsverket kan även titta på om det finns flera liknande händelser inrapporterade och undersöker sedan eventuella trender.
– Vi har möjlighet att stoppa en produkt, men för att det ska vara möjligt måste vi ha hårda data. Vi måste i så fall ha en bevisning som håller i en domstol, säger Henrik Johansson.